Nos choix alimentaires sont quotidiennement influencés, déterminés par notre perception du goût des aliments. Le goût est en réalité un phénomène plurimodal au cœur duquel l’olfaction (comprenant les odeurs et les arômes) joue un rôle essentiel. En effet, la perte de l’odorat engendrerait une perte de plaisir au sein de l’alimentation. Un dialogue s’effectue alors entre les régions olfactives et les régions cérébrales impliquées dans la prise alimentaire. Chez les personnes en surpoids ou souffrant d’obésité, nous pouvons observer un dysfonctionnement de l’odorat et une incapacité à réguler les odeurs qu’elles perçoivent. De manière générale, les odeurs alimentaires sont perçues comme étant plus agréables par les personnes affectées par l’obésité, celles-ci présentant pourtant une sensibilité plus faible à ces mêmes odeurs. De nombreux chercheurs tentent alors par le biais de diverses études de comprendre si le phénomène de dysfonctionnement olfactif est à l’origine du développement de l’obésité, ou si l’obésité elle-même engendre un tel trouble.
En quoi l’obésité peut-elle donc avoir un lien avec des changements olfactifs, de manière causale ou conséquentielle ?
Dans un premier temps nous allons nous porter sur ce qu’est l’obésité en tant que telle, puis nous allons nous intéresser au système olfactif et son fonctionnement. Enfin, nous tenterons d’expliquer le phénomène de dysfonctionnement olfactif chez les personnes souffrant d’obésité par le biais de plusieurs articles scientifiques.
I. Qu’est-ce que l’obésité ?
D’après l’Organisation mondiale de la santé (OMS), il faut savoir que :
• En 2016, environ 650 millions d'adultes (13% de la population totale) ainsi que 124 millions d'enfants et adolescents de 5 à 19 ans s’avéraient être obèses.
• En 2019, 38 millions d’enfants de moins de 5 ans souffraient déjà d’un surpoids ou de l’obésité.
Le surpoids et l’obésité sont alors définies comme étant une accumulation anormale ou excessive de graisse corporelle pouvant nuire à la santé d’un individu.
Les méthodes les plus largement utilisées pour mesurer le surpoids et l'obésité sont anthropométriques : elles concernent donc les mesures de la taille, de la masse corporelle, des plis sous-cutanés et de l'indice de masse corporelle (IMC).
L’IMC est une relation qui s'effectue entre le poids et la taille d’individu, soit : IMC = Poids (kg) / (Taille)² (m)
Cette relation permet notamment de classer l'obésité chez les adultes :
Un IMC supérieur ou égal à 30 kg / m² correspond à une situation d’obésité, et l’on parle d’obésité morbide lorsque l’IMC est supérieur ou égal 45 kg / m².
L'obésité est une maladie multifactorielle prenant notamment en compte des facteurs génétiques (voire épigénétiques) et environnementaux, mais aussi psychologiques. « Notamment » signifie que d’autres paramètres peuvent entrer en compte, telles que des causes métaboliques, physiologiques et hormonales, etc.
Ces facteurs environnementaux ont déclenché une augmentation radicale de l'obésité au cours des dernières décennies. Nous pouvons alors observer l’instauration d’un environnement obésogène, avec :
• Une nourriture abondante et palatable (riches en graisses saturées et en glucides raffinés/en sucres), dont l’accès est de plus en plus aisé.
• Des comportements sédentaires, où l’on passe donc bien plus de temps assis ou allongé que debout, et où la dépense physique se fait par conséquent de plus en plus faible. Cette sédentarité peut en partie être liée à l’urbanisation croissante (avec l’utilisation passive de transports en commun par exemple, avec un accès bien plus direct aux choses), aux avancées technologiques qui nous demandent toujours moins d’efforts, au contexte relatif à notre exercice professionnel (par exemple lorsque l’on travail dans un bureau toute la journée), et à bien d’autres raisons encore.
Diverses conséquences peuvent survenir suite au développement de l’obésité, telles que l’apparition du diabète de type 2, d’une résistance à l’insuline, de maladies cardiovasculaires, de cancers (du sein, des ovaires, de la prostate, du foie, du colon etc.), d’hypertension artérielle, d’athérosclérose, mais aussi de troubles musculosquelettiques (arthrose), etc.
Notons d’ailleurs que l’obésité peut être associée à des troubles du comportement alimentaire comme la boulimie et l’hyperphagie, dont les causes sont également multifactorielles.
Intéressons-nous maintenant au fonctionnement du système olfactif en tant que tel.
II. Le système olfactif et son fonctionnement.
Il faut savoir que l’on peut détecter des milliers d’odeurs. L’odorat, ou système olfactif est impliqué dans la perception et le traitement des informations des molécules odorantes. Divers facteurs peuvent influencer la détection des odeurs, tels que des facteurs génétiques, environnementaux, physiologiques et émotionnels, mais cela dépend également de l’état hormonal ou encore de l’âge de l’individu.
Lors de la respiration, les molécules odorantes atteignent la muqueuse qui se situe dans la zone postéro-dorsale des fosses nasales. Il existe deux voies d’accès à cette muqueuse olfactive, qui sont complémentaires :
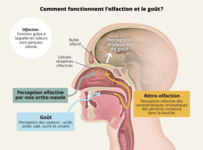
• La voie ortho-nasale (odeurs)
• La voie rétro-nasale (arômes se trouvant au niveau de la bouche et remontant vers les fosses nasales)
Quel trajet vont ensuite effectuer ces odeurs ?
En fait, les molécules odorantes vont venir se lier aux récepteurs olfactifs de la muqueuse. Ces récepteurs comportent des cils qui vont avoir pour rôle de capter ces molécules odorantes.
Une transduction olfactive va alors s’effectuer, c’est-à-dire que le signal chimique transmis par les cellules odorantes va être transformé en signal électrique, ce qui va produire un message nerveux informatif. Ce phénomène est appelé « codage de l’information ».
Ensuite, cette information va passer du nerf olfactif aux glomérules situés dans le bulbe olfactif, aboutissant alors à l’établissement d’une chimiotopie olfactive. C’est-à-dire qu’une « carte d’identité chimique des odeurs » va être dressée. Autrement dit, celle-ci va permettre de discriminer les diverses odeurs les unes des autres.
Enfin, les axones des neurorécepteurs du bulbe olfactif vont former un tractus olfactif (transmettant donc l’information olfactive) qui va se diriger vers le cortex olfactif primaire (ou cortex piriforme). Le lien entre bulbe olfactif et cortex olfactif primaire va alors permettre la mémorisation des odeurs mais aussi de faire un lien avec le comportement des individus.
En effet, le cortex olfactif est notamment relié à l’amygdale (jouant un rôle dans la régulation et le traitement des émotions), à l’hippocampe (essentiel à la consolidation des informations apprises et au rappel des souvenirs), à l’hypothalamus (important dans le maintien de l’homéostasie, et notamment au niveau de la prise alimentaire) et enfin au cortex orbitofrontal (impliqué dans les fonctions exécutives et la régulation du comportement).
Notons d’autre part que pour détecter une odeur, il faut dépasser un certain seuil, et que ce seuil dépend des personnes. Certains troubles olfactifs peuvent altérer la perception de ces odeurs. En effet, 5% de la population générale serait anosmique et 15% souffrirait d’hyposmie. L’anosmie concerne la perte totale de l’odorat, tandis que l’hyposmie est caractérisée par une baisse, une diminution quantitative du seuil olfactif, se traduisant par un déficit partiel de l’odorat. Ces troubles vont donc amener à une modification du comportement alimentaire.
Passons donc à quelques études mettant en évidence le lien entre ces troubles olfactifs et l’obésité.
III. Le dysfonctionnement de l’odorat chez les personnes souffrant d’obésité
1. L'hyposmie dans l'obésité
Dans une revue systématique, Mohammed et al. (2015) ont pu déterminer que :
• 54,3% de personnes obèses étaient hyposmiques (en comparaison, seulement 6,44% des personnes anorexiques l’étaient)
• Les participants ayant un IMC > 45 (obésité morbide) sont plus susceptibles de présenter un dysfonctionnement olfactif que les participants ayant un IMC < 45.
Cela suggèrerait donc qu’un dysfonctionnement olfactif puisse apparaître avec l’augmentation de l’IMC.
Une autre étude, citée dans cette revue, a permis d’établir le fait qu'un dysfonctionnement olfactif pouvait contribuer à la progression de l'obésité : en effet, des changements métaboliques internes entreraient en jeu.
Un dysfonctionnement olfactif affecterait donc le comportement alimentaire et un possible lien s'exercerait alors entre une altération de l'odorat et une alimentation excessive.
2. Lien entre hyposensibilité, désinhibition du comportement alimentaire et IMC
Nous allons maintenant nous focaliser sur une étude de Sophie Kindleysides et al. (2017) examinant le lien entre la sensibilité gustative, la sensibilité olfactive aux acides gras et la désinhibition du comportement alimentaire.
Notons avant tout quelques définitions utiles pour une meilleure compréhension de ce qui va suivre :
• La désinhibition est la tendance à trop consommer (= manger) en réponse à différents stimuli (c’est-à-dire qu’il n’y a pas de résistance).
• L’hyposensibilité est relative à un manque de stimulations sensorielles, à un défaut de perception, au fait qu’il y ait peu ou pas de réaction aux stimuli sensoriels.
• A l’inverse, l’hypersensibilité est une réaction excessive aux stimuli sensoriels.
Expériences effectuées :
Résultats :
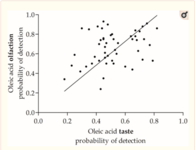
Cette première figure nous montre une corrélation positive entre le goût et la détection olfactive de l'acide oléique. C’est-à-dire que plus la détection olfactive de l’acide oléique est importante, plus le goût perçu de l’acide oléique sera également élevé.

Figure 2. Relation entre l'hypo- et l'hypersensibilité au goût de l'acide oléique, le taux de détection de l'olfaction, le seuil olfactif du n-butanol et le comportement alimentaire.
D’après ce tableau, les hyposensibles au goût de l’acide oléique auraient une sensibilité olfactive au n-butanol significativement plus faible.
On peut également constater une association entre hyposensibilité au goût des acides gras et comportement alimentaire désinhibé. Autrement dit, les sujets hyposensibles au goût des acides gras développent de manière significative un comportement alimentaire désinhibé et ont un IMC plus élevé.
↪ Le fait d’être hyposensible augmenterait la susceptibilité/le risque d’être en surpoids ou obèse de 3,4 fois par rapport à ceux qui ne sont pas hyposensibles.
De plus, les personnes hyposensibles détiendraient un pourcentage de graisse corporelle supérieur par rapport aux hypersensibles.
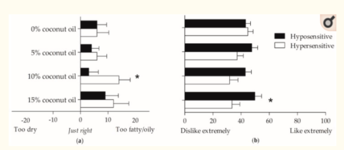
Figure 3. Relation entre l'hypo- et l'hypersensibilité gustative d'acide oléique, l'évaluation de la sensation en bouche et l'olfaction.
En outre, une corrélation s’exercerait entre la perception de la sensation en bouche de la crème riche en graisses et la sensibilité au n- butanol.
On peut plus particulièrement remarquer l’association d’une caractéristique « trop grasse/trop huileuse » avec une sensibilité olfactive plus élevée (soit une hypersensibilité).
Enfin, l’on peut observer que plus l’aliment est palatable (gras, ici), plus les hyposensibles l’apprécient.
Discussion/explications du phénomène :
Ce qu’il faut retenir :
3. La corrélation entre l’état de faim, la sensibilité olfactive et l’IMC
Puis, nous allons voir par le biais d’une étude menée par Lorenzo et al. (2010) que l’état de faim influencerait la sensibilité olfactive, et cela en fonction du type d’odeur (neutre ou alimentaire).
Objectifs :
Résultats :
Ce qu’il faut retenir :
Même lorsque les personnes ayant un IMC élevé se trouvent dans un état de satiété, les odeurs alimentaires restent pour elles appétentes. Elles continuent donc de consommer de la nourriture, les processus de régulation des odeurs et du contrôle de leur prise alimentaire étant altérés.
Pour finir, d’après une étude de Maria Poessel et al. (2020), des mécanismes hormonaux seraient impliqués dans l’altération du processus olfactif, et notamment ceux concernant l’Insuline.
Ce que l’on sait :
Dans la muqueuse olfactive se trouvent des récepteurs à diverses hormones telles que l’insuline, la leptine mais aussi la ghréline, etc. Ces hormones, suivant leur taux, vont entraîner différents signaux métaboliques qui vont permettre de déterminer la motivation quant à la recherche d’aliments, mais aussi le type d’aliment ainsi que la quantité consommée. Un certain nombre d’hormones jouent donc un rôle dans la régulation de notre métabolisme et de notre appétit.
Il existe différents types d’hormones :
L’insuline :
L’insuline est une hormone produite par les cellules β du pancréas, au niveau des îlots de Langherans. Il s’agit de la principale hormone de régulation de la glycémie dans l'organisme. Dans le cas d’une insulinorésistance (IR), les cellules normalement sensibles à l'action de l'insuline ne répondent plus correctement à l'action de l'hormone : le glucose n'entre plus suffisamment dans les cellules et la glycémie augmente alors.
Expériences :
Résultats :
Discussion :
Ce qu’il faut retenir :
Les personnes obèses présentent une hyposensibilité à l’olfaction, celle-ci étant reliée à un comportement désinhibé au cœur duquel le sujet réagira excessivement face à un stimulus (= prise alimentaire excessive). Il s’agit d’un processus de compensation au cœur duquel l’individu va augmenter la quantité ingérée afin de ressentir le même plaisir que celui initial, ce plaisir étant engendré par le goût.
L’individu va effectuer cette compensation en se tournant vers des aliments hyperpalatables (c’est-à-dire riches en graisses et en sucres)
Les personnes obèses présentent une acuité olfactive plus élevée pour les odeurs alimentaires lorsqu’ils se trouvent à l’état de satiété par rapport à l'état de non-satiété (= état de faim), ce qui entrave le processus de contrôle de la prise alimentaire.
Les changements hormonaux apparaissant au sein des personnes souffrant d’obésité pourraient expliquer la relation entre système olfactif et système endocrinien. Cela mènerait ainsi à la modification du régime alimentaire de l’individu et de la transformation interne des aliments.
Références :
En quoi l’obésité peut-elle donc avoir un lien avec des changements olfactifs, de manière causale ou conséquentielle ?
Dans un premier temps nous allons nous porter sur ce qu’est l’obésité en tant que telle, puis nous allons nous intéresser au système olfactif et son fonctionnement. Enfin, nous tenterons d’expliquer le phénomène de dysfonctionnement olfactif chez les personnes souffrant d’obésité par le biais de plusieurs articles scientifiques.
I. Qu’est-ce que l’obésité ?
D’après l’Organisation mondiale de la santé (OMS), il faut savoir que :
• En 2016, environ 650 millions d'adultes (13% de la population totale) ainsi que 124 millions d'enfants et adolescents de 5 à 19 ans s’avéraient être obèses.
• En 2019, 38 millions d’enfants de moins de 5 ans souffraient déjà d’un surpoids ou de l’obésité.
Le surpoids et l’obésité sont alors définies comme étant une accumulation anormale ou excessive de graisse corporelle pouvant nuire à la santé d’un individu.
Les méthodes les plus largement utilisées pour mesurer le surpoids et l'obésité sont anthropométriques : elles concernent donc les mesures de la taille, de la masse corporelle, des plis sous-cutanés et de l'indice de masse corporelle (IMC).
L’IMC est une relation qui s'effectue entre le poids et la taille d’individu, soit : IMC = Poids (kg) / (Taille)² (m)
Cette relation permet notamment de classer l'obésité chez les adultes :
Un IMC supérieur ou égal à 30 kg / m² correspond à une situation d’obésité, et l’on parle d’obésité morbide lorsque l’IMC est supérieur ou égal 45 kg / m².
L'obésité est une maladie multifactorielle prenant notamment en compte des facteurs génétiques (voire épigénétiques) et environnementaux, mais aussi psychologiques. « Notamment » signifie que d’autres paramètres peuvent entrer en compte, telles que des causes métaboliques, physiologiques et hormonales, etc.
Ces facteurs environnementaux ont déclenché une augmentation radicale de l'obésité au cours des dernières décennies. Nous pouvons alors observer l’instauration d’un environnement obésogène, avec :
• Une nourriture abondante et palatable (riches en graisses saturées et en glucides raffinés/en sucres), dont l’accès est de plus en plus aisé.
• Des comportements sédentaires, où l’on passe donc bien plus de temps assis ou allongé que debout, et où la dépense physique se fait par conséquent de plus en plus faible. Cette sédentarité peut en partie être liée à l’urbanisation croissante (avec l’utilisation passive de transports en commun par exemple, avec un accès bien plus direct aux choses), aux avancées technologiques qui nous demandent toujours moins d’efforts, au contexte relatif à notre exercice professionnel (par exemple lorsque l’on travail dans un bureau toute la journée), et à bien d’autres raisons encore.
Diverses conséquences peuvent survenir suite au développement de l’obésité, telles que l’apparition du diabète de type 2, d’une résistance à l’insuline, de maladies cardiovasculaires, de cancers (du sein, des ovaires, de la prostate, du foie, du colon etc.), d’hypertension artérielle, d’athérosclérose, mais aussi de troubles musculosquelettiques (arthrose), etc.
Notons d’ailleurs que l’obésité peut être associée à des troubles du comportement alimentaire comme la boulimie et l’hyperphagie, dont les causes sont également multifactorielles.
Intéressons-nous maintenant au fonctionnement du système olfactif en tant que tel.
II. Le système olfactif et son fonctionnement.
Il faut savoir que l’on peut détecter des milliers d’odeurs. L’odorat, ou système olfactif est impliqué dans la perception et le traitement des informations des molécules odorantes. Divers facteurs peuvent influencer la détection des odeurs, tels que des facteurs génétiques, environnementaux, physiologiques et émotionnels, mais cela dépend également de l’état hormonal ou encore de l’âge de l’individu.
Lors de la respiration, les molécules odorantes atteignent la muqueuse qui se situe dans la zone postéro-dorsale des fosses nasales. Il existe deux voies d’accès à cette muqueuse olfactive, qui sont complémentaires :

• La voie ortho-nasale (odeurs)
• La voie rétro-nasale (arômes se trouvant au niveau de la bouche et remontant vers les fosses nasales)
Quel trajet vont ensuite effectuer ces odeurs ?
En fait, les molécules odorantes vont venir se lier aux récepteurs olfactifs de la muqueuse. Ces récepteurs comportent des cils qui vont avoir pour rôle de capter ces molécules odorantes.
Une transduction olfactive va alors s’effectuer, c’est-à-dire que le signal chimique transmis par les cellules odorantes va être transformé en signal électrique, ce qui va produire un message nerveux informatif. Ce phénomène est appelé « codage de l’information ».
Ensuite, cette information va passer du nerf olfactif aux glomérules situés dans le bulbe olfactif, aboutissant alors à l’établissement d’une chimiotopie olfactive. C’est-à-dire qu’une « carte d’identité chimique des odeurs » va être dressée. Autrement dit, celle-ci va permettre de discriminer les diverses odeurs les unes des autres.
Enfin, les axones des neurorécepteurs du bulbe olfactif vont former un tractus olfactif (transmettant donc l’information olfactive) qui va se diriger vers le cortex olfactif primaire (ou cortex piriforme). Le lien entre bulbe olfactif et cortex olfactif primaire va alors permettre la mémorisation des odeurs mais aussi de faire un lien avec le comportement des individus.
En effet, le cortex olfactif est notamment relié à l’amygdale (jouant un rôle dans la régulation et le traitement des émotions), à l’hippocampe (essentiel à la consolidation des informations apprises et au rappel des souvenirs), à l’hypothalamus (important dans le maintien de l’homéostasie, et notamment au niveau de la prise alimentaire) et enfin au cortex orbitofrontal (impliqué dans les fonctions exécutives et la régulation du comportement).
Notons d’autre part que pour détecter une odeur, il faut dépasser un certain seuil, et que ce seuil dépend des personnes. Certains troubles olfactifs peuvent altérer la perception de ces odeurs. En effet, 5% de la population générale serait anosmique et 15% souffrirait d’hyposmie. L’anosmie concerne la perte totale de l’odorat, tandis que l’hyposmie est caractérisée par une baisse, une diminution quantitative du seuil olfactif, se traduisant par un déficit partiel de l’odorat. Ces troubles vont donc amener à une modification du comportement alimentaire.
Passons donc à quelques études mettant en évidence le lien entre ces troubles olfactifs et l’obésité.
III. Le dysfonctionnement de l’odorat chez les personnes souffrant d’obésité
1. L'hyposmie dans l'obésité
Dans une revue systématique, Mohammed et al. (2015) ont pu déterminer que :
• 54,3% de personnes obèses étaient hyposmiques (en comparaison, seulement 6,44% des personnes anorexiques l’étaient)
• Les participants ayant un IMC > 45 (obésité morbide) sont plus susceptibles de présenter un dysfonctionnement olfactif que les participants ayant un IMC < 45.
Cela suggèrerait donc qu’un dysfonctionnement olfactif puisse apparaître avec l’augmentation de l’IMC.
Une autre étude, citée dans cette revue, a permis d’établir le fait qu'un dysfonctionnement olfactif pouvait contribuer à la progression de l'obésité : en effet, des changements métaboliques internes entreraient en jeu.
Un dysfonctionnement olfactif affecterait donc le comportement alimentaire et un possible lien s'exercerait alors entre une altération de l'odorat et une alimentation excessive.
2. Lien entre hyposensibilité, désinhibition du comportement alimentaire et IMC
Nous allons maintenant nous focaliser sur une étude de Sophie Kindleysides et al. (2017) examinant le lien entre la sensibilité gustative, la sensibilité olfactive aux acides gras et la désinhibition du comportement alimentaire.
Notons avant tout quelques définitions utiles pour une meilleure compréhension de ce qui va suivre :
• La désinhibition est la tendance à trop consommer (= manger) en réponse à différents stimuli (c’est-à-dire qu’il n’y a pas de résistance).
• L’hyposensibilité est relative à un manque de stimulations sensorielles, à un défaut de perception, au fait qu’il y ait peu ou pas de réaction aux stimuli sensoriels.
• A l’inverse, l’hypersensibilité est une réaction excessive aux stimuli sensoriels.
Expériences effectuées :
- Evaluation du goût de l'acide oléique et des seuils d'olfaction de l’acide oléique, du seuil olfactif pour le n- butanol et évaluations subjectives de la sensation en bouche des échantillons de crème anglaise.
(L’acide oléique et le n-butanol sont des acides gras, ils constituent donc une catégorie des lipides, ceux-ci constituant notamment la matière grasse de notre organisme. C’est pourquoi ils sont étudiés dans ce contexte)
- Evaluation de l’apport alimentaire et du comportement alimentaire : questionnaire sur la fréquence des aliments (énergie, macronutriments, groupes alimentaires) et sur l'alimentation à trois facteurs (contention alimentaire cognitive, la désinhibition du contrôle et la sensibilité à la faim)
- Mesure de l’IMC et du pourcentage graisse corporelle
(L’acide oléique et le n-butanol sont des acides gras, ils constituent donc une catégorie des lipides, ceux-ci constituant notamment la matière grasse de notre organisme. C’est pourquoi ils sont étudiés dans ce contexte)
- Evaluation de l’apport alimentaire et du comportement alimentaire : questionnaire sur la fréquence des aliments (énergie, macronutriments, groupes alimentaires) et sur l'alimentation à trois facteurs (contention alimentaire cognitive, la désinhibition du contrôle et la sensibilité à la faim)
- Mesure de l’IMC et du pourcentage graisse corporelle
Résultats :
Cette première figure nous montre une corrélation positive entre le goût et la détection olfactive de l'acide oléique. C’est-à-dire que plus la détection olfactive de l’acide oléique est importante, plus le goût perçu de l’acide oléique sera également élevé.

Figure 2. Relation entre l'hypo- et l'hypersensibilité au goût de l'acide oléique, le taux de détection de l'olfaction, le seuil olfactif du n-butanol et le comportement alimentaire.
D’après ce tableau, les hyposensibles au goût de l’acide oléique auraient une sensibilité olfactive au n-butanol significativement plus faible.
On peut également constater une association entre hyposensibilité au goût des acides gras et comportement alimentaire désinhibé. Autrement dit, les sujets hyposensibles au goût des acides gras développent de manière significative un comportement alimentaire désinhibé et ont un IMC plus élevé.
↪ Le fait d’être hyposensible augmenterait la susceptibilité/le risque d’être en surpoids ou obèse de 3,4 fois par rapport à ceux qui ne sont pas hyposensibles.
De plus, les personnes hyposensibles détiendraient un pourcentage de graisse corporelle supérieur par rapport aux hypersensibles.

Figure 3. Relation entre l'hypo- et l'hypersensibilité gustative d'acide oléique, l'évaluation de la sensation en bouche et l'olfaction.
En outre, une corrélation s’exercerait entre la perception de la sensation en bouche de la crème riche en graisses et la sensibilité au n- butanol.
On peut plus particulièrement remarquer l’association d’une caractéristique « trop grasse/trop huileuse » avec une sensibilité olfactive plus élevée (soit une hypersensibilité).
Enfin, l’on peut observer que plus l’aliment est palatable (gras, ici), plus les hyposensibles l’apprécient.
Discussion/explications du phénomène :
• Relation entre la perception du goût de l'acide oléique et l'olfaction :
Il y aurait une association significative entre la capacité à détecter les acides gras et l'olfaction relative à ces acides gras.
Cela s’expliquerait en partie par l’existence de récepteurs jouant un rôle dans la détection du gras, nommés récepteurs CD36, se trouvant dans l’épithélium olfactif. Lorsque davantage de récepteurs CD36 s’expriment au sein d’un individu, celui-ci semblerait alors avoir une capacité de détection olfactive également plus élevée, et inversement.
• Perception du goût de l'acide oléique et comportement alimentaire désinhibé :
Une incapacité à détecter efficacement les graisses mènerait à une compensation de la satisfaction cognitive avec d'autres goûts, tels que le gras et le sucré, ce qui pourrait engendrer un poids supplémentaire sur le long terme.
• Perception du goût, olfaction et composition corporelle de l'acide oléique :
Une faible sensibilité (= hyposensibilité) au goût des graisses, et le lien entre goût et préférence pour les graisses seraient donc liés à un statut pondéral plus élevé (c’est-à-dire à un IMC plus élevé).
D’après une autre étude, nous pourrions en l’espace de 4 semaines augmenter de manière conséquente la sensibilité gustative à l’acide oléique par le biais d’un régime pauvre en graisses.
Il y aurait une association significative entre la capacité à détecter les acides gras et l'olfaction relative à ces acides gras.
Cela s’expliquerait en partie par l’existence de récepteurs jouant un rôle dans la détection du gras, nommés récepteurs CD36, se trouvant dans l’épithélium olfactif. Lorsque davantage de récepteurs CD36 s’expriment au sein d’un individu, celui-ci semblerait alors avoir une capacité de détection olfactive également plus élevée, et inversement.
• Perception du goût de l'acide oléique et comportement alimentaire désinhibé :
Une incapacité à détecter efficacement les graisses mènerait à une compensation de la satisfaction cognitive avec d'autres goûts, tels que le gras et le sucré, ce qui pourrait engendrer un poids supplémentaire sur le long terme.
• Perception du goût, olfaction et composition corporelle de l'acide oléique :
Une faible sensibilité (= hyposensibilité) au goût des graisses, et le lien entre goût et préférence pour les graisses seraient donc liés à un statut pondéral plus élevé (c’est-à-dire à un IMC plus élevé).
D’après une autre étude, nous pourrions en l’espace de 4 semaines augmenter de manière conséquente la sensibilité gustative à l’acide oléique par le biais d’un régime pauvre en graisses.
Ce qu’il faut retenir :
- Plus la capacité de détection d’une odeur est importante et plus le goût lié à cette odeur sera également détecté de manière élevée.
↪ Il s’exerce donc un lien entre perception olfactive et perception du goût, en particulier par rapport aux graisses
- Les personnes hyposensibles possèdent une sensibilité aux odeurs bien plus faible que les personnes non-hyposensibles. Leur perception du goût sera donc également plus faible, et le plaisir apporté par les aliments sera moindre. C’est pourquoi elles vont développer ce qu’on appelle un « comportement alimentaire désinhibé », c’est-à-dire qu’elles vont augmenter leur prise alimentaire pour chercher à ressentir un plaisir plus important, ce qui va les mener à ne plus pouvoir contrôler leur consommation alimentaire, à avoir tendance à ne plus savoir s’arrêter. A terme, cette prise alimentaire excessive peut mener à une prise de poids, c’est pourquoi l’on observe que les personnes hyposensibles ont globalement un IMC plus élevé que les personnes non-hyposensibles.
- Plus un aliment va être palatable (riche en graisses ou en sucre), plus les personnes hyposensibles vont apprécier cet aliment, parce qu’il va leur procurer davantage de plaisir. C’est l’inverse pour les personnes hypersensibles : plus l’aliment est palatable, plus il va leur être déplaisant car leur sensibilité olfactive est plus élevée que celle des hyposensibles.
⇒ Les habitudes alimentaires sont donc influencées par la perception du goût, et notamment par celle du goût des graisses.
3. La corrélation entre l’état de faim, la sensibilité olfactive et l’IMC
Puis, nous allons voir par le biais d’une étude menée par Lorenzo et al. (2010) que l’état de faim influencerait la sensibilité olfactive, et cela en fonction du type d’odeur (neutre ou alimentaire).
Objectifs :
- L’acuité olfactive (seuil et discrimination) varie-t-elle dans les différents états de la faim ?
- L’IMC peut-il influencer la sensibilité olfactive et celle-ci est-elle modulée par l'état de faim ?
- Test du seuil olfactif à une odeur neutre (Expériences 1 et 2)
- Test de discrimination à une odeur de nourriture : prise alimentaire avant et après tests (Expérience 2).
Expérience 1 :
- D’après ce graphique, la sensibilité olfactive pour une odeur neutre serait plus grande lorsque l’on se trouve dans un état de faim par rapport à l'état de satiété.
- De plus, cette sensibilité olfactive à une odeur neutre serait également plus importante dans un état de faim chez les personnes ayant un IMC faible par rapport aux personnes ayant un IMC élevé.
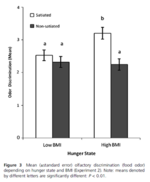
- Dans le cas d’une personne non-obèse, se trouver dans un état de satiété augmenterait la sensibilité olfactive, que les odeurs alimentaires soient associées ou non au repas consommé. Cette augmentation de la sensibilité olfactive observée sur le graphique de gauche se traduirait par le fait que les odeurs nous paraissent comme état plus désagréables du fait de l’état de satiété. Pour expliquer cela plus précisément, il faut savoir qu’après l’ingestion d’un repas s’exerce un phénomène qu'on appelle l'alliesthésie alimentaire négative. Il s'agit d'une baisse de la valeur hédonique olfactive d'un aliment après ingestion d'un repas. Cette valeur hédonique fait référence au plaisir que nous procure le fait de consommer des aliments. C’est pourquoi ces odeurs sont associées à quelque chose de désagréable.
- Les personnes ayant un IMC élevé posséderaient, elles, une acuité olfactive plus élevée pour les odeurs alimentaires à l'état de satiété par rapport à l'état de non-satiété (= à l’état de faim). Mais cette acuité olfactive augmente bien plus dans cet état de satiété par rapport aux personnes non-obèses. Cette augmentation va être due au fait que les odeurs alimentaires perçues par les sujets obèses restent particulièrement appétentes même après ingestion d’un repas à cause d’une mauvaise régulation de ces odeurs. Autrement dit, le phénomène d’alliesthésie alimentaire négative ne prend pas place, c’est-à-dire que la valeur hédonique des aliments ne diminuera pas, et les odeurs continueront d’être associées à quelque chose qui leur provoque du plaisir. Cela suggèrerait par conséquent un déficit du contrôle de la consommation de nourriture.
Même lorsque les personnes ayant un IMC élevé se trouvent dans un état de satiété, les odeurs alimentaires restent pour elles appétentes. Elles continuent donc de consommer de la nourriture, les processus de régulation des odeurs et du contrôle de leur prise alimentaire étant altérés.
4. Des mécanismes hormonaux sont impliqués dans l’altération du processus olfactifPour finir, d’après une étude de Maria Poessel et al. (2020), des mécanismes hormonaux seraient impliqués dans l’altération du processus olfactif, et notamment ceux concernant l’Insuline.
Ce que l’on sait :
Dans la muqueuse olfactive se trouvent des récepteurs à diverses hormones telles que l’insuline, la leptine mais aussi la ghréline, etc. Ces hormones, suivant leur taux, vont entraîner différents signaux métaboliques qui vont permettre de déterminer la motivation quant à la recherche d’aliments, mais aussi le type d’aliment ainsi que la quantité consommée. Un certain nombre d’hormones jouent donc un rôle dans la régulation de notre métabolisme et de notre appétit.
Il existe différents types d’hormones :
- Les hormones orexigéniques (ghréline, adiponectine) : celles-ci vont induire la stimulation de l'appétit et donc aussi, par conséquent, la prise alimentaire
- Les hormones anorexigéniques (insuline, leptine) : celles-ci vont induire le processus de satiété et réguler l'homéostasie énergétique sur le long terme.
L’insuline :
L’insuline est une hormone produite par les cellules β du pancréas, au niveau des îlots de Langherans. Il s’agit de la principale hormone de régulation de la glycémie dans l'organisme. Dans le cas d’une insulinorésistance (IR), les cellules normalement sensibles à l'action de l'insuline ne répondent plus correctement à l'action de l'hormone : le glucose n'entre plus suffisamment dans les cellules et la glycémie augmente alors.
Expériences :
- Mesure de la sensibilité à un aliment et à une odeur non alimentaire à l'état affamé ainsi qu’à l’état rassasié.
- Détermination de l'état de santé métabolique et de la réactivité hormonale en réponse à l'apport alimentaire : évaluation des niveaux pré et postprandiaux d'insuline, de leptine et de ghréline.
- Evaluation du poids corporel, de la taille et du tour de hanches.
Hypothèse : les hormones assurent la médiation des performances olfactives
Notons que l’outil « HOMA-IR » est une méthode de quantification de l’insulinorésistance (HOMA signifie : « Homeostasis Model Accessment of IR »).
Le groupe d’IMC noté « NW » signifie « non-obèse » ou « poids normal », le groupe « OW » signifie « surpoids » et le groupe « OB » est relatif à « l’obésité ».
La relation entre l'IMC et la sensibilité aux odeurs pour le chocolat serait médiée par des paramètres métaboliques de santé.
En effet, les valeurs relatives à l’insulinorésistance ainsi que les taux de leptine s’avéraient significativement plus élevés chez les personnes obèses, mais la sensibilité à ces hormones se révélait, elle, plus réduite.
De plus, chez les personnes obèses, les taux de ghréline totale s’avéraient également plus faibles.
• NW : « poids normal »
• OB : « obèse »
• OW : « surpoids »
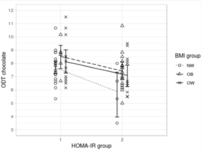
La sensibilité olfactive était plus élevée dans le groupe HOMA-IR optimal par rapport au groupe HOMA-IR élevé. On observe :
Figure 1. Relation entre la sensibilité aux odeurs de (ODT Chocolate), l'IMC (BMI) et l'IR (HOMA-IR).
Notons que l’outil « HOMA-IR » est une méthode de quantification de l’insulinorésistance (HOMA signifie : « Homeostasis Model Accessment of IR »).
Le groupe d’IMC noté « NW » signifie « non-obèse » ou « poids normal », le groupe « OW » signifie « surpoids » et le groupe « OB » est relatif à « l’obésité ».
La relation entre l'IMC et la sensibilité aux odeurs pour le chocolat serait médiée par des paramètres métaboliques de santé.
En effet, les valeurs relatives à l’insulinorésistance ainsi que les taux de leptine s’avéraient significativement plus élevés chez les personnes obèses, mais la sensibilité à ces hormones se révélait, elle, plus réduite.
De plus, chez les personnes obèses, les taux de ghréline totale s’avéraient également plus faibles.
Figure 2. Sensibilité aux odeurs de chocolat pour un groupe HOMA-IR optimal (HOMA-IR <1) et élevé (HOMA-IR> 1) pour différents groupes d’IMC.
Rappel :
• NW : « poids normal »
• OB : « obèse »
• OW : « surpoids »
La sensibilité olfactive était plus élevée dans le groupe HOMA-IR optimal par rapport au groupe HOMA-IR élevé. On observe :
- Une association semblerait positive entre l’IMC et la sensibilité olfactive lors du contrôle de l'IR.
- Une autre association, cependant négative, entre l'IR et la sensibilité olfactive vis-à-vis d’aliments et cela indépendamment de l'IMC.
- Plus l’IMC est élevé, plus la sensibilité aux odeurs du chocolat via l’IR est faible (« via » signifie « médié par »).
- Plus l'IMC est élevé, plus l'IR et les taux de leptine sont élevés.
- Plus l'IR est élevé, plus la sensibilité aux odeurs est faible, et cela indépendamment de l'IMC.
- Plus la masse de graisse viscérale est importante, plus la sensibilité aux odeurs alimentaires est faible (mécanisme une fois de plus médié par l’IR).
• Corrélation faiblement négative entre la ghréline totale et l'IMC :
Dans l’obésité, la réponse de la ghréline à l’apport alimentaire est atténuée. Ce qui expliquerait le fait que le niveau de ghréline pourrait alors ne pas diminuer correctement après un repas. Etant donné que cette hormone stimule l’appétit, les personnes obèses peuvent alors ressentir un appétit élevé même après avoir mangé/être rassasiées.
⇒ Dans ce cas, la ghréline agit alors indépendamment des besoins physiologiques de l’individu.
De plus, ce faible taux de ghréline dans l’obésité serait lié à un mécanisme compensatoire du bilan énergétique positif prolongé, celui-ci représentant le fait que l’énergie absorbée dépasse la dépense énergétique et ceci sur un temps relativement long. C’est ce qui mène alors à la prise de poids.
Par ailleurs, une autre hypothèse concernait le rapport entre la forme acylée (active, nommée AG) et la forme non acylée (inactive, nommée UAG) de la ghréline. En effet, dans le cas de l’obésité, ce rapport se révèlerait élevé d’après d’autres études. Cela signifierait donc que le niveau d’UAG serait moindre par rapport à celui de l’AG, ce qui expliquerait d’autant plus le fait que les personnes obèses continuent de ressentir un appétit important et donc une envie de consommer et cela même après avoir déjà pris un repas. Cependant, cette relation n’a pas pu être mise en évidence dans l’étude examinée actuellement. Mais c’est une piste qu’il faut continuer à étudier.
• Lien entre taux de leptine et obésité :
Dans le cas de l’obésité, des taux élevés de leptine (hormone de la satiété) seraient associés à une résistance à la leptine. Plusieurs mécanismes peuvent expliquer ce phénomène de résistance. Tout d’abord, celle-ci pourrait être liée à l’hyperinsulinémie (lorsque la production d'insuline par le pancréas dépasse la norme) et à la résistance à l’insuline. En effet, il y aurait une corrélation positive entre les taux de leptine et d’insuline (à jeun, pour les deux) au sein de l’obésité.
Mais celle-ci peut aussi s’expliquer par d’autres processus :
- Par une perturbation ou un blocage de la signalisation dans l’hypothalamus ;
- Des perturbations du transport de la leptine à travers la barrière hémato-encéphalique ;
- Une diminution de la sensibilité ou du nombre de récepteurs à la leptine.
Dans l’obésité, la réponse de la ghréline à l’apport alimentaire est atténuée. Ce qui expliquerait le fait que le niveau de ghréline pourrait alors ne pas diminuer correctement après un repas. Etant donné que cette hormone stimule l’appétit, les personnes obèses peuvent alors ressentir un appétit élevé même après avoir mangé/être rassasiées.
⇒ Dans ce cas, la ghréline agit alors indépendamment des besoins physiologiques de l’individu.
De plus, ce faible taux de ghréline dans l’obésité serait lié à un mécanisme compensatoire du bilan énergétique positif prolongé, celui-ci représentant le fait que l’énergie absorbée dépasse la dépense énergétique et ceci sur un temps relativement long. C’est ce qui mène alors à la prise de poids.
Par ailleurs, une autre hypothèse concernait le rapport entre la forme acylée (active, nommée AG) et la forme non acylée (inactive, nommée UAG) de la ghréline. En effet, dans le cas de l’obésité, ce rapport se révèlerait élevé d’après d’autres études. Cela signifierait donc que le niveau d’UAG serait moindre par rapport à celui de l’AG, ce qui expliquerait d’autant plus le fait que les personnes obèses continuent de ressentir un appétit important et donc une envie de consommer et cela même après avoir déjà pris un repas. Cependant, cette relation n’a pas pu être mise en évidence dans l’étude examinée actuellement. Mais c’est une piste qu’il faut continuer à étudier.
• Lien entre taux de leptine et obésité :
Dans le cas de l’obésité, des taux élevés de leptine (hormone de la satiété) seraient associés à une résistance à la leptine. Plusieurs mécanismes peuvent expliquer ce phénomène de résistance. Tout d’abord, celle-ci pourrait être liée à l’hyperinsulinémie (lorsque la production d'insuline par le pancréas dépasse la norme) et à la résistance à l’insuline. En effet, il y aurait une corrélation positive entre les taux de leptine et d’insuline (à jeun, pour les deux) au sein de l’obésité.
Mais celle-ci peut aussi s’expliquer par d’autres processus :
- Par une perturbation ou un blocage de la signalisation dans l’hypothalamus ;
- Des perturbations du transport de la leptine à travers la barrière hémato-encéphalique ;
- Une diminution de la sensibilité ou du nombre de récepteurs à la leptine.
Ce qu’il faut retenir :
- La sensibilité olfactive est plus faible quand l’IR est importante, en plus du fait que cette sensibilité olfactive soit plus faible quand l’IMC est élevé.
- L’IR et les taux de leptine augmentent de plus en plus au fur et à mesure que l’IMC lui-même augmente, mais la sensibilité à ces hormones est plus faible (c’est-à-dire que les cellules de l’individu ne répondent plus correctement, et de manière très faible, à l’expression de ces hormones). Ce taux élevé de leptine peut notamment être associé à une résistance à la leptine. Etant donné que la leptine est une hormone jouant un rôle dans la satiété, lorsqu'une résistance à cette hormone prend place, le processus de satiété ne s'effectue plus comme il le devrait, ce qui favorise la sensation de faim.
- Après un repas pris par une personne dont l’IMC est important, la ghréline, hormone stimulant la prise alimentaire, ne diminue pas comme on devrait l’observer chez des sujets « sains » et « non-obèses ». C’est pourquoi les personnes obèses peuvent ressentir un appétit encore élevé même en se trouvant dans un état de satiété.
Les personnes obèses présentent une hyposensibilité à l’olfaction, celle-ci étant reliée à un comportement désinhibé au cœur duquel le sujet réagira excessivement face à un stimulus (= prise alimentaire excessive). Il s’agit d’un processus de compensation au cœur duquel l’individu va augmenter la quantité ingérée afin de ressentir le même plaisir que celui initial, ce plaisir étant engendré par le goût.
L’individu va effectuer cette compensation en se tournant vers des aliments hyperpalatables (c’est-à-dire riches en graisses et en sucres)
Les personnes obèses présentent une acuité olfactive plus élevée pour les odeurs alimentaires lorsqu’ils se trouvent à l’état de satiété par rapport à l'état de non-satiété (= état de faim), ce qui entrave le processus de contrôle de la prise alimentaire.
Les changements hormonaux apparaissant au sein des personnes souffrant d’obésité pourraient expliquer la relation entre système olfactif et système endocrinien. Cela mènerait ainsi à la modification du régime alimentaire de l’individu et de la transformation interne des aliments.
- Les personnes étant affectées par un trouble olfactif/dysfonctionnement olfactif (tel que l’hyposmie) peuvent donc être sujettes au développement de l’obésité puisque des processus de compensation se mettront en place.
- A l’inverse, les personnes développant l’obésité subissent également des modifications olfactives internes et continues ce qui pourrait aboutir à l’apparition d’un dysfonctionnement olfactif à terme.
- Un dysfonctionnement olfactif peut également mener à une progression de l’obésité (obésité morbide)
Références :
- Lorenzo D. Stafford and Kimberley Welbeck. 2010. « High Hunger State Increases Olfactory Sensitivity to Neutral but Not Food Odors. » Chem. Senses 36: 189–198. https://doi.org/10.1093/chemse/bjq114
- Maria Poessel, Jessica Freiherr, Kathleen Wiencke, Arno Villringer, Annette Horstmann. 2020. « Insulin Resistance Is Associated with Reduced Food Odor Sensitivity across a Wide Range of Body Weights. » Nutrients 12(8), 2201. https://doi.org/10.3390/nu12082201
- Mohammed A. Islam, Ana B. Fagundo, Jon Arcelus, Zaida Agüera, Susana Jiménez-Murcia, José M. Fernández-Real, Francisco J. Tinahones, Rafael de la Torre, Cristina Botella, Gema Frühbeck, Felipe F. Casanueva, José M. Menchón and Fernando Fernandez-Aranda. 2015. « Olfaction in eating disorders and abnormal eating behavior : a systematic review. » Frontiers in psychology. https://doi.org/10.3389/fpsyg.2015.01431
- Sophie Kindleysides, Kathryn L. Beck, Daniel C. I. Walsh, Lisa Henderson, Shakeela N. Jayasinghe, Matt Golding, and Bernhard H. Breier. 2017. « Fat Sensation: Fatty Acid Taste and Olfaction Sensitivity and the Link with Disinhibited Eating Behaviour. » Nutrients 9(8): 879. https://doi.org/10.3390/nu9080879
Pièces jointes
Dernière édition: